OZON
KYSLÍK A JEHO FORMY
Kyslíkový atom se vyskytuje v přírodě v různých formách.
- Volná částice O, vysoce reaktivní a nestabilní (není radikál).
- Kyslík O2 . Tato forma je nejvíce rozšířena, je stabilní, bezbarvá jako plyn a bleděmodrá jako tekutina. Kyslík v této formě je pro život nezbytný, ale při nevhodných reakcích může být pro organismus toxický. Hraje významnou roli v oxidačních reakcích, které probíhají ve čtyřech krocích Feltonovy reakce. Při dostatku energie je výsledným produktem oxidace živin, CO2 a H2O . Při nedostatku energie tato reakce neproběhne úplně a vzniká velké množství volných radikálů a kyselých metabolitů. Tyto látky vyvolávají v biologických systémech oxidační stres. Oxidační stres není nedostatek kyslíku, ale nedostatek volné energie pro oxidaci.
- Kyslík O3 (ozon). Je reaktivní a nestabilní (není radikál). Ve své molekule má velký přebytek energie. Poločas rozpadu je velmi malý (desítky minut). Je běžně přítomný ve vzduchu a to v poměru 1 díl O3 na 10 milionů dílů vzduchu tj. asi 140ug/m3.
- Kyslík O4. Je velmi nestabilní molekula a rychle se rozpadá na 2 molekuly O2.
- Některé práce dokazují, že při složitých reakcích atomy kyslíku vytváří na velmi krátkou dobu molekuly kyslíku O8 a O64 .
OZON
Ozon je plyn s charakteristickým zápachem, respektive vůní, jakou můžeme cítit ve vzduchu po typické letní bouřce. Lidský čich je na tuto vůni obzvláště citlivý a je proto schopen zaregistrovat již i velmi malé a naprosto neškodné koncentrace tohoto plynu ve vzduchu.
 Poprvé byl tento plyn popsán Martinusem van Marumem holandským učencem (1750 - 1837).
Poprvé byl tento plyn popsán Martinusem van Marumem holandským učencem (1750 - 1837).

Při pokusech s elektrostatickou elektřinou na svých strojích roku 1785 popsal tak zvanou " vůni elektřiny " která která vzniká kolem elektrických strojů, pravděpodobně vlivem jejich jiskření.
 Roku 1840 prof. F. C. Schonbein ve své knize " Erzeugung des Ozons auf chemischem Wege " popsal proměnu vzdušného kyslíku působením elektrického výboje na plyn s charakteristickým zápachem. Tento plyn nazval podle řeckého slova ozein -
Roku 1840 prof. F. C. Schonbein ve své knize " Erzeugung des Ozons auf chemischem Wege " popsal proměnu vzdušného kyslíku působením elektrického výboje na plyn s charakteristickým zápachem. Tento plyn nazval podle řeckého slova ozein -  - ozon - vydávat vůni
- ozon - vydávat vůni
 V roce 1857 sestrojil Werner von Siemens přístroj, s jehož pomocí lze ozon vyrábět. Podle něj nazvaná trubice pracuje na principu tichého elektrického výboje.
V roce 1857 sestrojil Werner von Siemens přístroj, s jehož pomocí lze ozon vyrábět. Podle něj nazvaná trubice pracuje na principu tichého elektrického výboje.
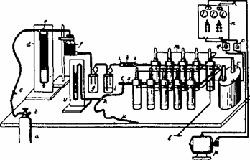 První přístroje schopné praktického užití jsou ze začátku 20. století.
První přístroje schopné praktického užití jsou ze začátku 20. století.
OZON V NÁS A OKOLO NÁS
V našem těle vznikají při reakcí vody s kyslíkem peroxidy a uvolňuje se ozon.
H2O + 2O2 = H2O2 + O3Při rozpadu 2 mol O3 vznikají 3 mol O2 a uvolní se energie, která je využita při oxidačních reakcích.
O3 + O3 = 3O2 + 286 kJOrganismus umí tuto formu kyslíku metabolizovat a využívat. Je pro život stejně důležitý jako stopové prvky.
Ve volné přírodě vzniká ozon několika způsoby :
-
Působením elektrického výboje - blesku při bouřce.

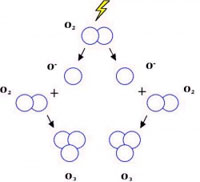

Takto jednorázově vzniklé množství ozonu se rozptýlí v ovzduší a postupně rozloží. Způsobí vznik typické bouřkové " vůně ".
-
Působením UV záření ve stratosféře.

Stratosféra se rozkládá ve výšce 15 - 50 km nad povrchem naší planety.
Ve výšce 20 - 30 km se vlivem UV záření tvoří ozon.
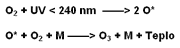
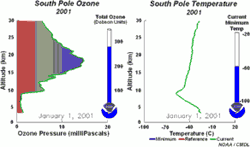
Tento Ozon klesá dolů (je těší než vzduch) a dochází k jeho postupnému rozpadu. Za normálních podmínek jsou tyto procesy v rovnováze. Střední hodnota koncentrace ozonu je více méně konstantní 4 - 5 ppm. Její maximální hodnota dosahuje 10 ppm. Této oblasti se říká ozonová vrstva (Ozonosféra). Hodnota koncentrace ozonu je mnohokrát větší než u povrchu země kde dosahuje hodnoty 0,03 - 0,04 ppm.
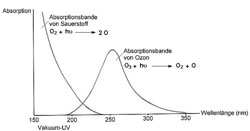
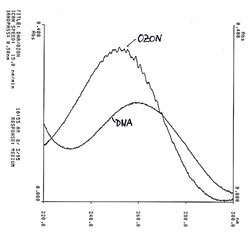
Ochranná vrstva ozonu se chová jako filtr. Absorbuje podstatnou část UV záření (Harleyovo pásmo v oblasti UV záření 250 nm) a představuje účinnou ochranu rostlin a živočichů na zemi před tímto zářením.
Porušení této vrstvy má za následek zvýšení intenzity UV záření na povrchu země, které ovlivňuje genetické procesy vzhledem k absorbci tohoto spektra UV záření DNA řetězci. Tím může dojít k mutaci DNA a zvýšení výskytu genetických, kožních a očních problémů u lidí, úhynu planktonu v mořích, ovlivnění fotosyntézy rostlin a narušení životně důležitých potravinových řetězců.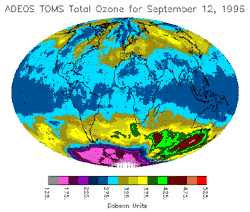

Ozonová vrstva je narušována průmyslovým znečišťováním. Mezi nejnebezpečnější znečištovatele patří fluorchlorované uhlovodíky, které jsou velmi stabilní a stoupají do stratosféry. Tyto sloučeniny se používají především jako chladiva v ledničkách, mrazničkách, klimatizačních zařízeních a jako hnací plyny v různých sprejích. Stav ozonové vrstvy nad celou naší planetou je neustále monitorován.
-
Fotochemickou reakcí vyvolanou UV zářením mezi uhlovodíky výfukových a odpadních plynů, oxidů dusíku v přízemní vrstvě atmosféry (troposféře).
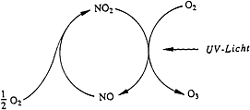
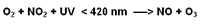
Koncentrace tohoto ozonu je úměrná znečištění přízemní vrstvy atmosféry. Koncentraci ozonu umíme přesně změřit a tím určit velikost znečištění. Velikost znečištění se udává množstvím ozonu v přízemní vrstvě. Tento ozon nacházející, se v těsné blízkosti zemského povrchu, je mediálně z neznalosti někdy označován jako nebezpečný. Nebezpečné jsou ale vyšší koncentrace oxidů dusíku a uhlovodíků které způsobují vážné zdravotní potíže.
VLASTNOSTI CHARAKTERISTIKA
Ozon je světlemodrý plyn s charakteristickým zápachem těžší než vzduch. Jeho molekula je tvořena třemi atomy kyslíku.
Chemická značka O3 .
Je velmi nestabilní a poměrně rychle se rozkládá na kyslík O2 . Při teplotě 20° C , tlaku 101,3 kPa je poločas rozpadu 45 minut.
Při teplotě 30° C a stejném tlaku je poločas rozpadu jen 20 minut.
Ozon není radikál. Má velmi silné oxidační schopnosti je reaktivnější než kyslík.
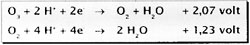
Fyzikálně chemické vlastnosti ve srovnání s kyslíkem
| ozon | kyslík | |
|---|---|---|
| chemická značka | O3 | O2 |
| bod tání | -192,5°C | -218°C |
| bod varu | -111,9°C | -182,7°C |
| molekulární váha | 48 | 32 |
| úhel vazby | 127° | - |
| vzdálenost vazby | 0,126 / 0,224 nm | 0,121 nm |
| dipólový moment | 0,55 Debye | 0 |
| magnetické vlastnosti | diamagnetický | paramagnetický |
| hmotnost při 0°C, 1 atm = 101,3 kPa (vzduch 1,29 g/litr) | 2,143 g/litr | 1,429 g/litr |
| rozpustnost ve 100 ml H2O při 0°C , 101,3 kPa | 49,4 ml (106 mg) | 4,91 ml (7 mg) |
| přebytek energie při 0°C, 1 atm =101,3 kPa | 142 kJ/Mol | 0 |
| elektrický potenciál | 2,07 V | 1,23 V |
Ozon má dvě spektrální absorpční pásma. Harleyovo pásmo v oblasti UV záření 250 nm s velmi velkým útlumem (E = 6000 m2/kg) a Cappuisovo pásmo v oblasti 600 nm (oranžová) s malým útlumem (E =3 m2/kg).
Koncentrace ozonu ve směsi plynů se udává množstvím O3 v jednotce objemu směsi
mg/m3 , µg/ml , 1 mg/m3 = 0,001µg / 1 ml
nebo poměrnou částí O3 k celkovému množství
ppm - parts per milion (miliontá část) 1 ppm = 0,0001 %
Pro směs ozonu (O3) a vzduchu platí 1 mg/m3 = 0,467 ppm .
Pro směs ozonu (O3) a kyslíku (O2) platí 1 mg/m3 = 0,455 ppm ,
1 µg/ml = 455 ppm .
VYUŽITELNÉ VLASTNOSTI OZONU
Svou vysokou oxidační schopností má nezastupitelné místo v chemickém průmyslu.Oxidací likviduje vysokomolekulární sloučeniny, chlorované bifenyly, organické sloučeniny, jedovaté aromatické látky, kyanidy, fenoly, síru, železo, mangan. Detoxikační schopností likviduje karcinogeny. Silný dezodorizační efekt způsobuje rozrušení zapáchajících látek a tím redukci zápachu a chuti. Vysoká rozpustnost v tekutinách a krátký poločas rozpadu umožňuje vysoké sycení kyslíkem. Baktericidní, virucidní a antimykotické vlastnosti se využívají k desinfekci při úpravě vody, v potravinářském a farmateutickém průmyslu. Desinfekční vlastnosti jsou udávány likvidací nejrezistentnějšího Echoviru 12 do 12 minut.
V lékařské praxi se využívá vlastností ozonu k léčbě poruch prokrvení, virových, bakteriálních a mykotických onemocnění, k aktivaci imunitního systému. Moderní transfúzní stanice využívají ozon ke sterilizaci krevních konzerv, jako dokonalý nástroj proti přenosu viru hepatitidy a HIV.
TECHNICKÝ OZON
Technický ozon je směs vzduchu a ozonu připraveného z atmosférického vzduchu, nebo technického kyslíku. Je používán hlavně pro úpravu vody a v chemickém průmyslu.
LÉKAŘSKÝ OZON
Lékařský ozon je směs medicinálního kyslíku a ozonu připraveného z medicinálního kyslíku. Přístroj pro výrobu lékařského ozonu musí zajistit požadovanou koncentraci a dávku. Rozsah koncentrace pro lékařské aplikace je 1 - 100 mikrogramů ozonu (O3) na 1 mililitr směsi (µg/ml), tomu odpovídá poměr 0.05 % - 5 % O3 k 99.95 % - 95 % O2 . Ozonová molekula není stabilní, jeho lékařská forma musí být připravená na místě užití.
OZON - HYGIENICKÉ POŽADAVKY
Lidský čich je schopen rozeznat přítomnost ozonu ve vzduchu již při velmi nízkých koncentracích od 10 µg/m3 O3. Tato schopnost je však individuální a v trvalé přítomnosti nízkých koncentrací ozonu se poměrně rychle ztrácí.
Při nízkých koncentracích <cca 110 µg/m3 má ozon sladkou, příjemnou vůni.
Při delším pobytu v místech se zvýšenou koncentrací ozonu (nad cca 350 µg/m3) se dostavuje pálení očí, v nosu a v krku, v některých případech i tlak na hrudi, kašel a bolest hlavy.
Nejvíce citliví jsou na ozon lidé, kteří mají zdravotní obtíže, jako je astma, chronické problémy dýchacích cest a nemoci oběhové soustavy.
Při koncentracích ozonu vyšších než cca 1100 µg/m3 jsou silně drážděny oči a horní cesty dýchací, dostavují se bolesti hlavy.
Koncentrace vyšší než cca 2150 µg/m3 způsobí během několika minut silné dráždění sliznice dýchacích cest, bronchospasmatické stavy a kašel.
Koncentrace nad 21 000 µg/m3 mají v závislosti na době expozice za následek bezvědomí, krvácení z plic a posléze smrt.
Při vdechování větší koncentrace ozonu dochází k poškození řasinkového epitelu průdušek.
PŘÍPUSTNÉ LIMITY KONCENTRACE OZONU
Nař. vlády ČR č. 178/2001 Sb. stanovuje přípustný expoziční limit (PEL) 100 µg/m3, který nesmí být překročen v celosměnném průměru. Krátkodobé překročení je možné až do hodnoty NPK-P. Hodnota NPK-P, tj. nejvyšší přípustná koncentrace, která nesmí být překročena v žádném případě, činí 200 µg/m3.
Vyhl. MZ č. 6/2002 Sb., stanoví hygienické limity chemických, fyzikálních a biologických ukazatelů pro vnitřní postředí pobytových místností některých staveb. Limitní hodinová koncentrace ozonu byla stanovena na 100 µg/m3.
KONCENTRACE OZONU V PŘÍZEMNÍ VRSTVĚ ATMOSFÉRY
Podle výsledků dlouhodobého projektu hygienické služby - Monitoringu zdravotního stavu obyvatelstva - se v ČR pohybují koncentrace ozonu v přízemní vrstvě atmosféry v letním období mezi 60 až 120 µg/m3, maximální (hodinové) hodnoty však mohou dosáhnout nebo přesáhnout osmihodinový imisní limit, tj. 180 µg/m3. V zimním období se tyto hodnoty pohybují okolo 30 až 60 µg/m3.
Obecně je vyšších dlouhodobých průměrných hodnot dosahováno ve venkovských a horských oblastech, kde však nedochází k jejich lokálním výrazným nárůstům. Ozon zde vzniká v důsledku přirozeného fotochemického cyklu v přízemní vrstvě atmosféry . V oblastech s vyšší nadmořskou výškou je vznik ozonu podporován vyšší intenzitou slunečního záření. Ve velkých městských aglomeracích je ozonu v důsledku jeho reakcí s přítomnými oxidy dusíku méně, a dlouhodobé průměrné hodnoty jsou proto nižší. Při vhodných podmínkách však může nastat "ozonová epizoda" (vznik fotochemického smogu v průmyslových a městských aglomeracích) s nárůstem koncentrace ozonu v ovzduší, který může trvat několik dní. V jejich průběhu mohou koncentrace přesahovat 200 µg/m3. Dle směrnic EU musí být obyvatelstvo informováno o překročení 180 µg/m3 a varováno při překročení 360 µg/m3.
Navigace
Akce a aktuality
- Neplátce DPH. (10.1.2023)
Od 1. 1. 2023 nejsme plátci DPH. [ celá zpráva ] - Změna adresy firmy ! (1.1.2016)
Nová adresa [ celá zpráva ] - KNIHOVNA 2013 (21.2.2014)
pro uživatele TAO 80 [ celá zpráva ]
... a další právě probíhající akce si prohlédněte v sekci [ akce a aktuality ]
